Brustkrebs / Mammakarzinome
1. Antihormonelle Therapie
2. Trastuzumab (Herceptin ®)
3. Bisphosphonate
1. Antihormonelle Therapie /
Weibliche
Geschlechtshormone können das Wachstum von Brustkrebs fördern. Voraussetzung
hierfür ist, dass an der Oberfläche der Tumorzellen Eiweißstoffe (sogenannte
Hormonrezeptoren) vorhanden sind, an die die weiblichen Geschlechtshormone
binden können. Bei etwa zwei Drittel der Patientinnen mit Brustkrebs (Mammakarzinom) finden sich solche Hormonrezeptoren an der
Tumorzelloberfläche. Diese werden durch den Pathologen bei der mikroskopischen
Untersuchung des Tumormaterials routinemäßig mitbestimmt. Unterschieden wird
zwischen Rezeptoren für Östrogen (engl. „Estrogen“)
(Estrogenrezeptor; ER) und Progesteron
(Progesteronrezeptor; PR). Bei Nachweis von
Hormonrezeptoren (entweder ER oder PR oder beide) kann eine gegen diese Hormone
gerichtete antihormonelle Behandlung erfolgen.
Weibliche
Geschlechtshormone werden vor der Menopause vorwiegend in den Eierstöcken
(Ovarien) produziert. Aber auch nach der Menopause, also nach Beendigung der
regelmäßigen Menstruationszyklen, werden weiterhin Östrogene gebildet. Diese
entstehen durch Umwandlung anderweitig im Körper gebildeter Hormone
(Androgene). An dieser Umwandlung sind in vielen Körpergeweben vorhandene
Enzyme beteiligt, die als Aromatasen bezeichnet
werden.
Als
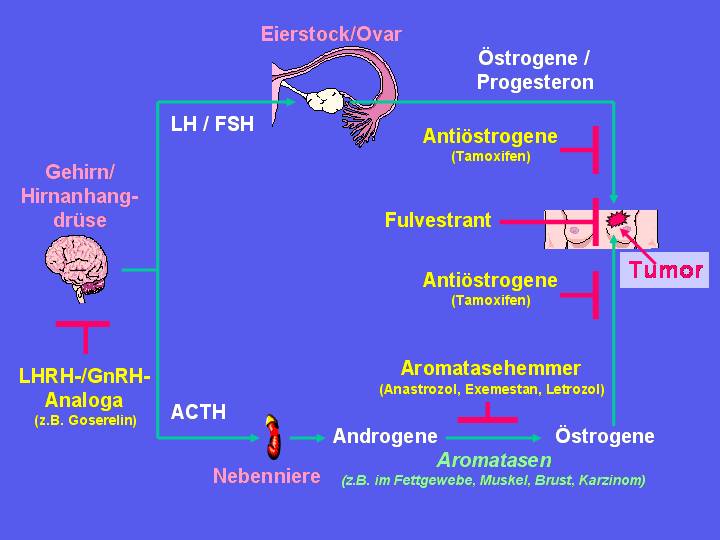
antihormonelle Behandlung kommen grundsätzlich folgende Maßnahmen in Betracht: (siehe
auch Abbildung 1):
1. Ausschaltung der Eierstöcke (Ovarien):
Diese
Maßnahme kann bei jüngeren Patientinnen mit erhaltenem Menstruationszyklus,
also vor der Menopause (prämenopausale Patientinnen),
durchgeführt werden. Früher erfolgte die Ausschaltung der Eierstocksfunktion
durch Operation oder Bestrahlung. Heute werden hierzu Medikamente verwendet,
die an der Hirnanhangsdrüse wirken und dort die Freisetzung eines Hormons
(LHRH) unterbinden, das die Eierstöcke zur Produktion von Geschlechtshormonen
(Östrogene, Progesteron) anregt. Diese Medikamente
werden als LHRH-Analoga oder GnRH-Analoga
bezeichnet und werden entweder monatlich oder 3-monatlich als Medikamentendepot
unter die Haut gespritzt.
2. Hemmung der Östrogenbindung am Östrogenrezeptor:
Das
bekannteste, seit Jahrzehnten in klinischen Einsatz befindliche Medikament ist Tamoxifen. Es wird in Tablettenform einmal täglich, meist
in einer Dosis von 20 mg, eingenommen.
3. Hemmung der Östrogenproduktion durch Hemmung der Aromatasen (Aromatase-Hemmstoffe;
Aromataseinhibitoren):
Hierzu
stehen verschiedene Medikamente zur Verfügung: Anastrozol
(Arimidex®), Letrozol (Femara®) und Exemestan (Aromasin®). Es handelt sich hierbei um Aromataseinhibotoren
(AI) der 3. Generation. Unterschieden werden diese entsprechend ihrer
chemischen Struktur in sogenannte nicht-steroidale (Anastrozol, Letrozol) und steroidale (Exemestan) Aromatasehemmer. Diese Medikamente werden einmal täglich in
Tablettenform eingenommen.
4. Abbau des Östrogenrezeptors:
Seit
wenigen Monaten steht hierzu auch in Deutschland das Medikament Fulvestrant (Faslodex®) zur
Verfügung. Fulvestrant wirkt als Antiöstrogen und
führt zu einem vermehrten Abbau des Östrogenrezeptors. Es wird einmal monatlich
intramuskulär (in einen Muskel) injiziert.
Wann werden diese antihormonellen Behandlungsformen angewendet ?
Es
ist prinzipiell zu unterscheiden zwischen einer Sicherheits-/Vorsorgebehandlung
(adjuvante Therapie) nach erfolgter Operation und
einer Behandlung bei Nachweis von Tochtergeschwülsten (Metastasen).
Von
einer (adjuvanten) Medikamentenbehandlung
spricht man nach der lokalen Behandlung des Brusttumors (durch Operation und
Bestrahlung), wenn Tochtergeschwülste (Metastasen) zwar nicht nachweisbar sind,
das Risiko eines Tumorrückfalls jedoch gesenkt werden soll. Bei der Behandlung
des Brustkrebs wird in vielen Fällen eine adjuvante
Behandlung mit einer sogenannten Chemotherapie, einer antihormonellen Therapie
oder beidem empfohlen. Die Empfehlung, welche Art der adjuvanten
Behandlung sinnvoll ist, richtet sich nach dem Rückfallrisiko. Dieses kann
heute anhand einer Vielzahl von Ergebnissen aus klinischen Studien recht gut
geschätzt werden. Hierzu stehen auch Computerprogramme zur Verfügung, mit denen
die Wahrscheinlichkeit der Verringerung des Rückfallrisikos durch Chemotherapie
und antihormonelle Therapie berechnet werden kann.
Eine
zusätzliche oder alleinige adjuvante antihormonelle
Therapie wird immer dann empfohlen, wenn Hormonrezeptoren (ER und/oder PR;
siehe oben) auf den Tumorzellen nachweisbar sind. Bei prämenopausalen
Patientinnen kommen hierzu LHRH-Analoga (siehe oben),
gegebenenfalls in Kombination mit Tamoxifen, in
Betracht.
Welche Bedeutung hat eine Sicherheitsnachbehandlung bzw. eine adjuvante antihormonelle Therapie ?
Eine
antihormonelle Nachbehandlung, die bei postmenopausalen
Patientinnen bislang üblicherweise mit Tamoxifen
für 5 Jahre durchgeführt wurde, senkt das Rückfallrisiko um ca. 40-50% und
das Risiko, an den Folgen des Brustkrebs zu versterben, um ca. 20-30%. Je
nach Risiko bei der betroffenen Patientin verbessert sich die langfristige
Überlebenschance damit um ca. 5-10%.
Wie lange wird eine antihormonelle Behandlung als
Sicherheitsbehandlung (adjuvante Therapie) nach
Brustkrebs empfohlen ?
Die Gesamtdauer der antihormonellen Therapie bei postmenopausalen Patientinnen richtet sich derzeit danach, ob eine solche Therapie neu begonnen wird oder bereits eine Behandlung mit Tamoxifen durchgeführt wird.
Bislang
galt für postmenopausale Patientinnen eine Behandlungsdauer für
die Tamoxifeneinnahme von 5 Jahren. Durch die neuen
Studienergebnisse zu den Aromatasehemmern haben
sich diese Empfehlungen allerdings teilweise geändert (siehe unten), so dass
die Gesamtbehandlungsdauer je nach Vorbehandlungsdauer mit Tamxifen – entsprechend den jetzt vorliegenden Daten – bis
zu 10 Jahre betragen kann.
Bei
prämenopausalen Patientinnen wird eine Behandlung mit
einem LHRH-Analogon meist für eine Dauer von 2-3, ggfs. bis zu 5 Jahren empfohlen. Wird gleichzeitig Tamoxifen verordnet, beträgt die Behandlungsdauer mit Tamoxifen in der Regel 5 Jahre.
In welcher Reihenfolge werden Chemotherapie und antihormonelle
Therapie angewendet ?
Wenn
eine (adjuvante) Medikamentenbehandlung nach Operation
des Brusttumors empfohlen wird und keine Chemotherapie erfolgen soll, kann
die antihormonelle Therapie bereits mit der Bestrahlung (nach brusterhaltender
Operation) begonnen werden. Auf jeden Fall sollte sie nach Abschluß der Strahlenbehandlung begonnen werden (Abbildung
2).
Wird
eine zusätzliche Chemotherapie empfohlen, wird diese meist innerhalb von 4
Wochen nach der Brustoperation begonnen. Im Anschluss hieran kann die
antihormonelle Therapie – gegebenenfalls bereits zeitgleich mit der nach der
Chemotherapie stattfindenden Bestrahlung - eingeleitet werden. Chemotherapie
und antihormonelle Behandlung sollten allerdings nicht gleichzeitig
erfolgen.
Abbildung
2:
Reihenfolge der Behandlungsmaßnahmen
nach Brustkrebsoperation

Welche Bedeutung haben Aromatasehemmstoffe
(Aromataseinhibitoren) für die adjuvante
Behandlung ?
Aromataseinhibitoren
werden seit vielen Jahren für die Behandlung von Tochtergeschwülsten nach
Versagen einer antihormonellen Behandlung mit Tamoxifen
verwendet. Insofern ist der Nachweis ihrer Wirksamkeit bei der Behandlung
von Brustkrebs bereits seit langem erbracht. Daher wurden vor einigen Jahren
klinische Studien begonnen, in den geprüft wird,
ob Aromataseinhibitoren auch für die adjuvante
Behandlung geeignet sind. Inzwischen liegen die Ergebnisse aus einigen dieser
Studien vor, die
mit Anastrozol, mit Letrozol und mit
Exemestan durchgeführt wurden (Abbildung 3).
In
die Untersuchung mit Anastrozol (ATAC-Studie)
wurden über 9.000 Patientinnen einbezogen, die entweder Anastrozol
allein, Tamoxifen allein oder die Kombination beider
Medikamente erhielten. Die Behandlung mit Anastrozol
erwies sich der Therapie mit Tamoxifen bezüglich
des krankheitsfreien Überlebens als statistisch signifikant überlegen. Die
Häufigkeit von Brustkrebsrückfällen war im 5. Beobachtungsjahr bei den
mit Anastrozol behandelten Patientinnen um 3,3%
geringer als bei den mit Tamoxifen behandelten Patientinnen.
In
weiteren Untersuchung mit Anastrozol (ITA-Studie / ABCSG-8 / ARNO-95) wurde zunächst für 2-3 Jahre
Tamoxifen verabreicht. Anschließend erhielten die Patientinnen
bis zur Gesamtbehandlungsdauer von 5 Jahren entweder weiter Tamoxifen oder Anastrozol. Die bisherigen
Ergebnisse dieser Studie deuten ebenfalls darauf hin, dass die Folgebehandlung
mit Anastrozol die Rate von Brustkrebsrückfällen verringert.
In die Untersuchung (MA.17) mit Letrozol, die vom kanadischen Krebsforschungsinstitut (NCIC) geleitet wurde, wurden mehr als 5.000 postmenopausale Patientinnen einbezogen, die nach 5-jähriger Tamoxifen-Gabe für 5 Jahre entweder täglich Letrozol oder ein „Scheinpräparat“ (Plazebo) erhielten. Die Ergebnisse zeigen eine Verringerung von Brustkrebsrückfällen, wobei die Rate des krankheitsfreien Überlebens nach 4 Jahren mit Letrozol bei 93% und ohne Letrozol bei 87% lag. Dies entspricht nach 4 Jahren einem Vorteil bezüglich des krankheitsfreien Überlebens von 6% zugunsten der Patientinnen, die nach Tamoxifen Letrozol erhielten.
In
einer weiteren großen Untersuchung (BIG 1-98) wurden etwa 8000 Patientinnen
untersucht, die entweder 5 Jahre Tamoxifen, 5 Jahre Letrozol oder 2 Jahre
Letrozol gefolgt von 3 Jahren Tamoxifen oder 2 Jahre Tamoxifen gefolgt von
3 Jahren Letrozol erhielten.
In
die Untersuchung mit Exemestan (IES) wurden
ca. 4.700 Patientinnen einbezogen. Nach etwa 2-3-jähriger Tamoxifen-Einnahme
wurde die Behandlung bei der Hälfte der Patientinnen mit Tamoxifen
bis zu 5 Jahren fortgeführt. Die andere Hälfte der Patientinnen erhielt Exemestan. Die Gesamtbehandlungsdauer betrug 5 Jahre. Auch
in dieser Studie wurde ein Vorteil durch die Gabe des Aromataseinhibitors
Exemestan gesehen. Nach vorläufigen Ergebnissen
wurde das krankheitsfreie Überleben nach 3 Jahren von 86,8% mit Tamoxifen
allein um 4,7% durch Exemestan auf 91,5% verbessert.
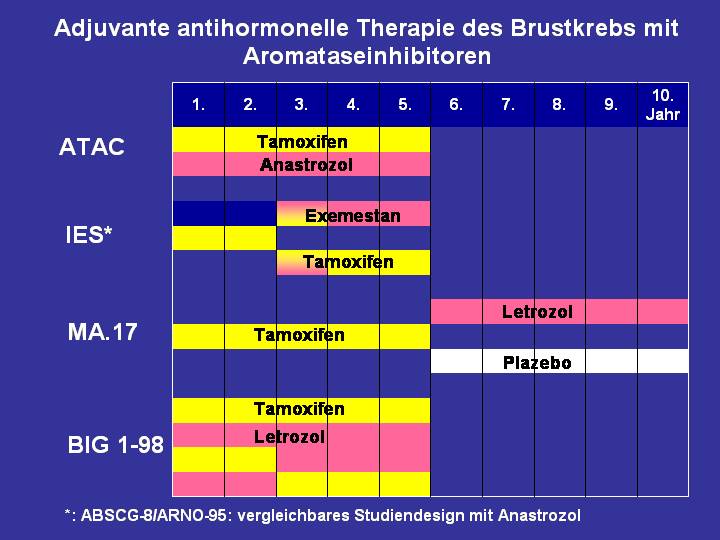
Gibt es Gruppen von Patientinnen, die von einem Aromatasehemmer eventuell mehr profitieren als andere ?
Solche
Unterschiede zu erkennen ist – mathematisch oder statistisch gesehen – sehr
schwierig. Mögliche Unterschiede, die nachträglich in Untersuchungen/Studien
gefunden werden, sollten üblicherweise die Entscheidungen zu einer bestimmten
Behandlung nicht beeinflussen und es gilt grundsätzlich, solche Ergebnisse
mit Vorsicht zu betrachten. Wissenschaftlich dienen solche Erkenntnisse aber,
um neue Fragen in neuen Studien zu klären.
So
gibt es beispielsweise Hinweise aus solchen Untersuchungen, dass Patientinnen
mit einem bestimmten Muster von Hormonrezeptoren auf den Tumorzellen (ER positiv/PR
negativ) eher von einem Aromatasehemmer als von
Tamoxifen profitieren könnten. Ferner gibt es Hinweise,
dass Aromatasehemmer bei Patientinnen mit einem
Tumor mit Vorhandensein des Eiweißstoffs (Rezeptors) HER-2/neu möglicherweise
besser wirksam sind als Tamoxifen.
Welche Nebenwirkungen haben Aromatasehemmstoffe
im Vergleich zu Tamoxifen ?
Da
die oben angeführten Studien mit Aromataseinhibitoren
bisher zumeist nur auf Ergebnissen einer ca. 2-4-jährigen Beobachtungszeit
beruhen, ist eine so exakte Sicherheitsbeurteilung, wie sie für Tamoxifen
getroffen werden kann, noch nicht möglich. Grundsätzlich ist zu bedenken,
dass Tamoxifen nicht nur ein Hemmstoff des Östrogenrezeptors ist,
sondern selbst auch an verschiedenen Organen wie ein Östrogen wirken kann.
Dieser Effekt kann mögliche Vorteile und auch Nachteile mit sich bringen.
So stabilisiert Tamoxifen beispielsweise die Knochen,
führt aber zu einer leichten Häufung von Gebärmutterkrebs, weshalb regelmäßige
diesbezügliche gynäkologische Kontrollen empfohlen werden. Zudem steigt u.a.
das Risiko von Gefäßkomplikationen gering an.
Aromatasehemmstoffe
andererseits führen zu einem reinen Östrogenentzug, weshalb andere Nebenwirkungen
auftreten können als bei Tamoxifen. Beachtung findet
dabei die Osteoporose (der verstärkte Knochenabbau), die bei Aromatasehemmern um einige Prozent häufiger auftritt als bei
Tamoxifen und etwas gehäuft zu Knochenbrüchen führen
kann. Das Risiko, an einem Gebärmutterkrebs zu erkranken, ist bei den o.g.
Aromatasehemmstoffen im Vergleich zu Tamoxifen nach bisherigen Ergebnissen offensichtlich verringert.
Dasselbe betrifft mögliche Gefäßkomplikationen (Thrombosen und Embolien),
die mit Aromatasehemmstoffen im Vergleich zu Tamoxifen
– nach bisherigen Ergebnissen - ebenfalls reduziert sind. Auch vaginale Blutungen
sind bei Einnahme von Aromatasehemmern etwas weniger
häufig als bei Tamoxifen. Bei etwa jeder vierten
bis dritten Patientin können jedoch Muskel- und Gelenkbeschwerden auftreten,
die allerdings jedoch auch in vergleichenden Untersuchungen ohne Behandlung
von zahlreichen Patientinnen berichtet werden.
Hieraus
ergibt sich nach den bisherigen Ergebnissen, dass Aromatasehemmer
vorteilhaft erscheinen bei denjenigen Patientinnen, die ein erhöhtes Risiko
für Gefäßkomplikationen. Das Risiko, mit einem Aromatasehemmer einen Knochenbruch
(Fraktur) zu erleiden, liegt um etwa 1-3% höher als bei Einnahme von
Tamoxifen. Auf Knochenprobleme ist daher besonders zu achten. Derzeit wird
in Studien untersucht, ob die gleichzeitige Gabe eines knochenstabilierenden
Medikaments (Bisphosphonate) die Nebenwirkungs-
bzw. Kompliaktionsrate an den Knochen verringern kann (siehe auch
weiter unten).
Zusammenfassende Schlussfolgerung zur adjuvanten
Therapie mit Aromatasehemmern:
Generell
sind die bisherigen Ergebnisse mit Aromatasehemmern
so ermutigend, dass diese für die Mehrzahl der Patientinnen bereits jetzt
von mehreren internationalen Fachgesellschaften empfohlen werden. Bei Patientinnen,
die derzeit noch Tamoxifen erhalten, ist entsprechend den oben genannten Ergebnissen
ein Wechsel von Tamoxifen auf einen Aromataseinhibitor zu erwägen.

Wird eine antihormonelle Behandlung evtl. auch vor einer Operation
verabreicht (präoperative oder neoadjuvante Behandlung) ?
Eine
klassische Chemotherapie wird häufig bereits vor der Operation des Brusttumors
durchgeführt, wenn eine brusterhaltende Operation zunächst nicht möglich
erscheint. Es konnte gezeigt werden, dass bei größeren Tumoren oder Tumoren mit
ungünstigem Sitz in der Brust nach einer solchen (präoperativen/neoadjuvanten) Chemotherapie häufiger eine brusterhaltende
Operation durchgeführt werden kann.
Dieses
Konzept wurde in einigen kleineren Untersuchungen auch mit einer
antihormonellen Behandlung geprüft. Dabei zeigte sich, dass der Tumor durch
eine solche Therapie bei jeder 3. bis 4. Patientin deutlich an Größe abnahm und
dass auch die Häufigkeit brusterhaltender Operationen zunahm. Im Vergleich mit
einer Chemotherapie war die Häufigkeit einer vollständigen Tumorrückbildung
jedoch deutlich geringer. Bisher gilt, dass eine antihormonelle präoperative Behandlung bei solchen Patientinnen in
Betracht kommen könnte, bei denen eine Chemotherapie kaum möglich ist, z.B.
wegen hohen Alters oder Begleiterkrankungen.
Welche antihormonelle Behandlung kommt in Betracht, wenn
Tochtergeschwülste (Metastasen) vorliegen ?
Wenn
nachgewiesen wurde, dass auf den Tumorzellen Hormonrezeptoren
(Östrogenrezeptoren / Progesteronrezeptoren)
vorhanden sind, kommen grundsätzlich alle Medikamente in Betracht, die die
Wirkung der Östrogene an den Tumorzellen verringern bzw. verhindern. Bei
Patientinnen vor der Menopause (prämenopausale Patientinnen)
kommen vorrangig LHRH-Analoga sowie Tamoxifen in Betracht. Bei Patientinnen nach der Menopause
(postmenopausale Patientinnen) kommen Tamoxifen, Aromatasehemmstoffe
und Fulvestrant in Betracht. Momentan ist noch nicht
abschließend geklärt, ob es eine beste Reihenfolge für die Anwendung dieser
Medikamente gibt. Traditionell wurde die Therapie bei postmenospausalen
Patientinnen mit Tamoxifen begonnen. Nachdem die
modernen Aromatasehemmstoffe entwickelt und geprüft
wurden, stellte sich heraus, dass diese auch dann noch eine Wirksamkeit
aufweisen können, wenn Tamoxifen nicht länger wirksam
ist. Die Aromatasehemmer wurden in der Folge dann
auch als erste antihormonelle Behandlung eingesetzt. Dabei fanden sich in
einigen Untersuchungen Vorteile zugunsten der Aromatasehemmer.
So ergab sich beispielsweise bei der Prüfung eines Aromatasehemmstoffes,
dass die Zeitdauer bis zur Notwendigkeit einer klassischen Chemotherapie im
Vergleich mit Tamoxifen deutlich verlängert war.
Ebenso wurde beschrieben, dass die Zeitdauer der Tumorkontrolle, d.h. der Zeit,
in der die Tumorerkrankung nicht fortschreitet, verlängert sein kann. In
jüngster Zeit kommt nun noch Fulvestrant hinzu, das
ebenso wie die Aromatasehemmer nach Versagen der
Behandlung mit Tamoxifen wirksam sein kann.
Ist nach Versagen der Behandlung mit einem antihormonellen
Medikament bereits eine Chemotherapie erforderlich oder können weitere
antihormonelle Therapien Erfolg haben ?
Durch
ihre teilweise unterschiedlichen Wirkmechanismen können antihormonelle Behandlungen
oftmals hintereinander eingesetzt werden. Wenn Tamoxifen
nicht mehr ausreichend wirkt, können Aromatasehemmer
oder Fulvestrant eingesetzt werden. Nach
Unwirksamwerden der Aromatasehemmer Anastrozol oder Letrozol können
der Aromatasehemmstoff Exemestan
oder Fulvestrant oder auch – falls zuvor noch nicht
verabreicht – Tamoxifen wirksam sein.
Die
Wirksamkeit einer Nachfolgetherapie kann bei einzelnen Patientinnen durch eine
Tumorverkleinerung gekennzeichnet sein. Meist ist aber eine Stabilisierung der
Tumorerkrankung zu beobachten, d.h. dass die Erkrankung zunächst nicht weiter
fortschreitet.
Die
Entscheidung, eine antihormonelle Folgetherapie zu wählen oder zu einer
klassischen Chemotherapie zu wechseln, hängt überwiegend davon ab, wie rasch der
Tumor fortschreitet und welche Beschwerden die Erkrankung verursacht. Bei
langsam fortschreitender Erkrankung kann ein Behandlungsversuch mit einer
antihormonellen Folgebehandlung sinnvoll sein. Falls die Tumorerkrankung
Beschwerden bereitet oder Probleme bevorstehen, wird aufgrund der höheren
Chance einer Chemotherapie, den Tumor bzw. die Tochtergeschwülste zu
verkleinern, die Entscheidung in Richtung einer Chemotherapie tendieren.
2. Antikörpertherapie mit Trastuzumab (Herceptin ®)
Bei
etwa jeder vierten bis fünften Patientin mit Brustkrebs findet sich auf den
Tumorzellen ein besonderer Eiweißstoff (Rezeptor), der – ähnlich wie die
Hormonrezeptoren – für die Behandlung genutzt werden kann. Dieser Rezeptor wird
„HER-2“ oder „neu“ genannt, abgekürzt oft HER-2/neu. Dieser Rezeptor wird heute
routinemäßig vom Pathologen bei der Untersuchung des Tumors mitbestimmt.
Unterschieden wird hierbei in 3 Stufen des Nachweises: 1+, 2+ oder 3+. Die
Stufe 3+ bedeutet, dass der HER-2/neu-Rezeptor
vorhanden und für eine Behandlung möglicherweise genutzt werden kann. Die Stufe
1+ bedeutet, dass der Rezeptor nicht ausreichend vorhanden ist. Wird eine Stufe
2+ beschrieben, ist eine Spezialuntersuchung erforderlich um zu klären, ob die
Tumorzellen diesen Rezeptor aufweisen oder nicht.
Wird
der HER-2/neu-Rezeptor nachgewiesen, kann im
Bedarfsfall eine Behandlung mit einem sogenannten Antikörper erfolgen. Dieser
Antikörper (Trastuzumab; Handelsname Herceptin) kann an der Außenseite der Tumorzelle an diesen
Rezeptor binden und bei einem Teil der Patientinnen zu einem Tumorzelluntergang
bzw. zu einer Tumorverkleinerung führen.
Der
Antikörper Trastuzumab (Herceptin) kann einmal pro Woche, alle 2 oder 3 Wochen als
Infusion verabreicht werden. Je nach Wahl des begleitenden Chemotherapiemedikaments
wird dieses ebenfalls wöchentlich oder alle 3 Wochen verabreicht. Die endgültige
Wahl der Behandlungsart wird im Gespräch mit dem behandelnden Onkologen entschieden.
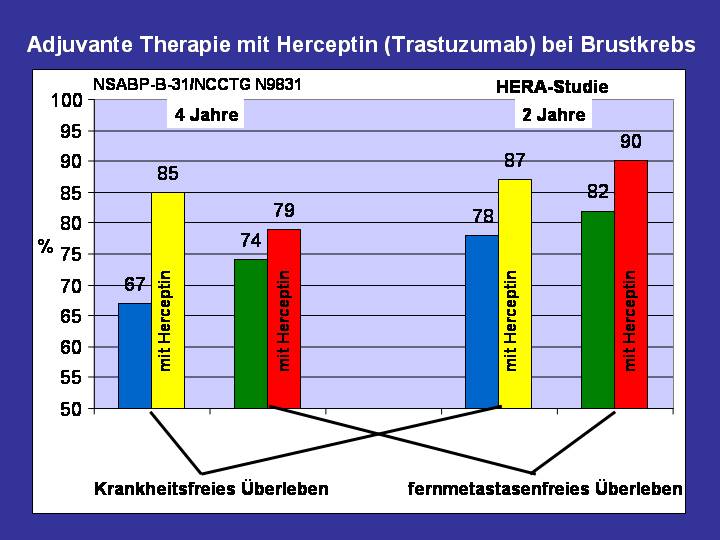
So wurde in einer gemeinsamen Auswertung von 2 US-amerikanischen Untersuchungen gezeigt, dass die Wahrscheinlichkeit, ohne Brustkrebsrückfall zu überleben, nach 4 Jahren 67% ohne zusätzliches Herceptin und 85% mit Herceptin beträgt. Auch die Wahrscheinlichkeit, ohne Fernmetastasen zu überleben, wurde durch Herceptin von von 74% auf 79% erhöht. Die Gesamtchance, nach 4 Jahren zu überleben, wurde durch Herceptin um ca. 4% erhöht.
In der europäischen HERA-Studie beträgt die Nachbeobachtungszeit derzeit nur etwa 2 Jahre. Trotz dieser kurzen Zeitdauer zeigte sich jedoch auch hier ein Vorteil durch Herceptin für das krankheitsfreie und fernmetastasenferie Überleben.
Für
die 3 oben genannten Untersuchungen gilt, dass längere Nachbeobachtungszeiten
abzuwarten sind um herauszufinden, ob die genannten Vorteile auch langfristig
Bestand haben.
Abbildung 5: Adjuvante Zusatztherapie mit oder ohne Herceptin bei Brustkrebspatientinnen
3. Bisphosphonate
Bisphosphonate
sind Medikamente, die den Knochenabbau hemmen. Bisphosphonate
werden daher beispielweise zur Behandlung oder zur Vorbeugung der Osteoporose,
dem meist altersbedingten Knochenschwund, eingesetzt. Daneben führen auch
viele Tumoren zu einem verstärkten Knochenabbau (Abbildung 6).
Dieser
tumorbedingte Knochenabbau kann zum Zusammenbruch bzw. zum Sintern von Kochen
und damit zu zahlreichen Problemen führen. An der Wirbelsäule kann dies zu
„Wirbelbrüchen“ – zu Frakturen – führen; an Röhrenknochen (z.B. am
Oberschenkel) können Knochenbrüche / Frakturen u.a. Operationen zur Folge
haben. In vielen Fällen führen solche Knochensinterungen bzw. Knochenbrüche zu
Schmerzen oder anderweitigen Einschränkungen der Lebensqualität, z.B. durch
Operationen, Krankenhausaufenthalte, etc. Häufig sind auch langwierige,
mehrwöchige Strahlentherapien (Bestrahlungsbehandlungen) die Folge, die die
Tumorzellen im Knochen abtöten und den betroffenen Knochen stabilisieren
sollen.
Abbildung 6: Tumorbedingter Knochenabbau durch Aktivierung
von Knochenzellen, den Osteoklasten.
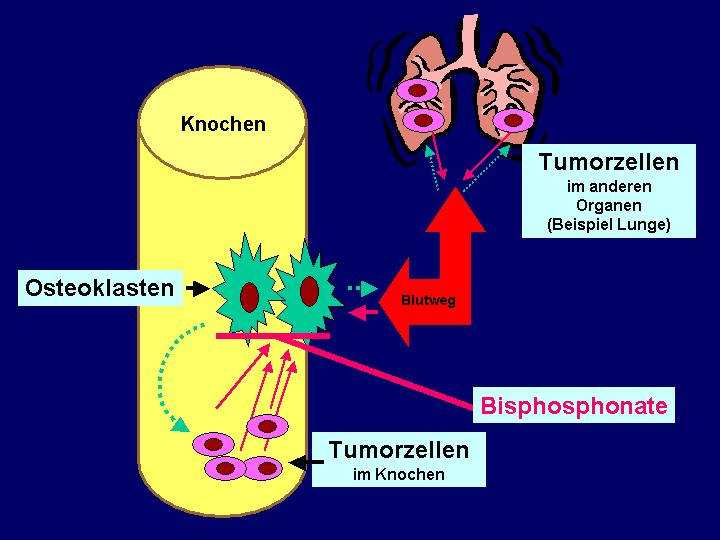
Die knochenabbauenden Zellen (Osteoklasten) werden angeregt durch Eiweißstoffe (rote
Pfeile), die von den Tumorzellen im Knochen in Nachbarschaft der Osteoklasten vorhanden sind. Zusätzlich können solche
Eiweißstoffe auch von Tumorzellen in anderen Organen über das Blut zu den Osteoklasten gelangen (rote Pfeile). Gleichzeitig können
die Osteoklasten und andere Zellen Eiweißstoffe
produzieren, die bei einzelnen Tumoren die Tumorzellvermehrung fördern (grüne
Pfeile). Bisphosphonate hemmen die Aktivität der Osteoklasten und führen somit zu einer Verringerung des
Knochenabbaus.
Bereits
seit vielen Jahren ist bekannt, dass Bisphosphonate
zu einer Verringerung von Knochenkomplikationen bei Tumorerkrankungen führen.
Dies gilt beispielsweise für Brustkrebserkrankungen, für das Plasmozytom (multiple Myelom;
eine Erkrankung weißer Blutkörperchen, der Plasmazellen)
und das Prostatakarzinom.
Wann
werden Bisphosphonate routinemäßig eingesetzt ?
Bisphosphonate
werden üblicherweise dann eingesetzt, wenn Tumorabsiedlungen im Knochen (Knochenmetastasen;
ossäre Metastasen) bekannt sind. In zahlreichen
Untersuchungen wurde nachgewiesen, dass die regelmäßige Gabe / Einnahme von
Bisphosphonaten die Häufigkeit von Komplikationen
senkt; Wirbelkörper- und andere Knochenbrüche sind seltener, die Notwendigkeit
von Strahlenbehandlungen, Schmerzen, Operationen und Krankenhausaufenthalten
nimmt ab. Insgesamt wird die Häufigkeit von Knochenkomplikationen um ca. 30%
gegenüber der Gabe eines „Scheinpräparats“ (Plazebo) gesenkt.
Wie
werden Bisphosphonate verabreicht ?
Bei
Patientinnen mit Bruskrebs und Knochenmetastasen
stehen folgende hochwirksame Bisphosponate zur
Verfügung: Zoledronsäure (Zoledronat;
Zometa ®), Ibandronat (Ibandronsäure; Bondronat ®) und Pamidronat (Pamidronsäure; Aredia ®). Clodronat, ein Bisphosphonat, das üblicherweise in Tablettenform
verabreicht wird, hat nicht durchweg zu so eindeutigen Verbesserungen gegenüber
Plazebo (Scheinpräparaten) geführt wie die o.g.
Medikamente und wird daher nicht mehr von allen internationalen
Fachgesellschaften (Leitlinien) empfohlen. Zoledronat
und Pamidronat werden als Infusionen alle 3-4 Wochen
verabreicht. Ibandronat steht seit wenigen Monaten
auch in Tablettenform zur Verfügung.
Zoledronat und Ibandronat weisen in einigen vorklinischen Untersuchungen
teilweise eine höhere Wirksamkeit auf als Pamidronat,
weswegen die erstgenannten Medikamente Pamidronat
teilweise abgelöst haben. Als Vorteil der erstgenannten Medikamente (Zoledronat, Ibandronat) gilt
auch, dass diese als kürzere Infusion (Zoledronat:
ca. 15 Minuten; Ibandronat: ca. 1 Stunde) verabreicht
werden als Pamidronat (ca. 2-3 Stunden). Die kürzere
Infusionszeit wird vielfach als praktikabler und seitens der Patienten als
angenehmer empfunden.
Falls
Bisphosphonate in Tablettenform eingenommen werden,
müssen besondere Verhaltensmaßnahmen vor, während und nach Einnahme beachtet
werden, unter anderem um Reizungen im Rachen, in der Speiseröhre und im
Magen-Darm-Trakt vorzubeugen.
Wie
lange werden Bisphosphonate verabreicht ?
Sofern
Knochenmetastasen nachgewiesen sind, gilt allgemein, daß
Bisphosphonate fortwährend verabreicht werden
sollten.
Welche
Nebenwirkungen haben Bisphosphonate ?
Meist sind Bisphosphonate auch bei langfristiger, mehrjähriger
Verabreichung sehr gut verträglich.
Gelegentlich können nach
der (ersten) Infusion grippeähnliche Beschwerden (geringes Fieber, Schwäche,
Kopfschmerzen) oder Muskelbeschwerden auftreten. Abhängig von der
Infusionsgeschwindigkeit und der Dosis können bei verschiedenen Bisphosphonaten auch Nierenfunktionsstörungen auftreten.
Diese Nebenwirkung ist jedoch recht selten. Darüber hinaus können
Erniedrigungen der Blutwerte für Kalzium, Magnesium und Phosphor auftreten.
Diese Veränderungen sind in der Regel jedoch ohne weitere Auswirkungen und
Bedeutung.
Bisphosphonate, die in
Tablettenform eingenommen werden, können zu „Magen-Darm“-Beschwerden
führen. Wichtig ist die korrekte Einnahme wie im Beipackzettel beschrieben.
Sollte die Einnahme wegen aufgetretener Beschwerden oder der Unpässlichkeiten,
die bei der Einnahme zu berücksichtigen sind, nicht sichergestellt sein,
empfiehlt sich der Wechsel auf eine etwa 4-wöchentliche intravenöse Gabe
(Infusionen).
Haben
Bisphosphonate bei Patientinnen mit Bruskrebs ebenso wie die antihormonelle Therapie und die
Chemotherapie eine Bedeutung als adjuvante Therapie,
d.h. als „Sicherheitstherapie“ ?
Diese
Frage wird derzeit in großen Studien untersucht. Bisher gibt es einige
Ergebnisse, die vermuten lassen, dass Bisphosphonate
als „Sicherheitstherapie“ (adjuvante Therapie) – d.h.
wenn mit bildgebenden Verfahren keine Knochenmetastasen nachgewiesen wurden –
sinnvoll sein könnten. Eine offizielle Empfehlung zu einer solchen Therapie
wurde aufgrund der bisherigen Daten allerdings noch nicht ausgesprochen. Die
Gründe hiefür liegen in teilweise unterschiedlichen Ergebnissen, kleinen
Patientenzahlen und anderen Kritikpunkten am Studienaufbau bzw. der
Studiendurchführung. Mehrheitlich wurden diese Untersuchungen mit dem Bisphosphonat Clodronat
durchgeführt. Dabei wurde ein Teil der Patientinnen mit einem Scheinpräparat (Plazebo) behandelt, die andere Hälfte der Patientinnen
erhielt das Bisphosphonat (z.B. täglich 1600 mg Clodronat in Tablettenform).
In einer der Untersuchungen wurden 302 Patientinnen untersucht,
bei denen mit besonders aufwendigen, sorgfältigen Untersuchungen vereinzelte
Tumorzellen im Knochenmark (Mikrometastasen) nachgewiesen wurden. Nach einer
Beobachtungsdauer von 5 Jahren fand sich bei den mit Clodronat
behandelten Patientinnen eine Verringerung von Knochenmetastasen und anderen
Organmetastasen, einhergehend mit einer Verbesserung der Überlebenschance. Nach
einer Beobachtungsdauer von 103 Monaten (ca. 8 ½ Jahre) findet sich in einer
aktuellen Analyse von 2004 kein signifikanter Unterschied mehr hinsichtlich
Knochenmetastasen und anderen Organmetastasen; auch fand sich kein (statistisch
signifikanter) Unterschied hinsichtlich des krankheitsfreien Überlebens;
interessanterweise war die Überlebenschance der Patientinnen, die mit Clodronat behandelt wurden, allerdings weiterhin höher als
bei den restlichen Patientinnen.
In einer skandinavischen Studie wurden 299 Patientinnen mit
Brustkrebs und Lymphknotenbefall behandelt, die entweder Clodronat
für eine Zeitdauer von 3 Jahren oder Plazebo
erhielten. Die Häufigkeit von Knochenmetastasen war in beiden Patientengruppen
vergleichbar; Patientinnen, die Clodronat erhielten,
wiesen in dieser Untersuchung häufiger Organmetastasen und ein geringeres
krankheitsfreies Überleben auf als Patientinnen, die kein Clodronat
erhielten. Ein Überlebensvorteil zugunsten der Patientinnen, die mit Clodronat behandelt wurden, fand sich nicht.
In einer dritten Untersuchung aus Großbritannien wurden über einen
Zeitraum von 11 Jahren insgesamt 1069 Patientinnen mit unterschiedlichen
Stadien von Brustkrebs (ohne und mit Lymphknotenbeteiligung) und
unterschiedlicher adjuvanter Tumortherapie behandelt.
Eine Hälfte der Patientinnen erhielt Clodronat über
einen Zeitraum von 2 Jahren. Nach einer Beobachtungszeit von 2 und 5 Jahren
fanden sich eine Verringerung von Knochenmetastasen und eine Verbesserung der
Überlebenschance für die Patientinnen, die Clodronat
erhalten hatten.
In einer kleinen Untersuchung aus Japan wurden 90 Patientinnen mit
Brustkrebs und mindestens 4 Lymphknotenmetastasen zur Hälfte mit Pamidronat behandelt. Dabei fand sich eine Verringerung der
Häufigkeit von Knochenmetastasen bei den mit Pamidronat
behandelten Patientinnen. Die Häufigkeit anderweitiger Organmetastasen war
nicht nennenswert verringert.
Insgesamt
deuten einige Ergebnisse aus diesen Studien darauf hin, dass Bisphosphonate eine gewisse Bedeutung für die adjuvante Behandlung bei Patientinnen mit erhöhtem Risiko
für Knochen erlangen könnten. Bevor diese Ergebnisse jedoch nicht in großen
Studien, die derzeit durchgeführt werden, bestätigt werden, werden Bisphosphonate als adjuvante Behandlung
bisher nicht generell empfohlen.
4. Adjuvante medikamentöse Therapie (vor oder nach der Operation; adjuvante antihormonelle Therapie / adjuvante oder neoadjuvante Chemotherapie)
Was bedeutet "neoadjuvante" oder "adjuvante" Chemotherapie ?
Eine
adjuvante Therapie wird durchgeführt, um das Rückfallrisiko zu verringern.
Der Begriff "adjuvant" leitet sich ab vom Lateinischen "adjuvare"


5. Medikamentöse Therapie bei Nachweis von Metastasen
Sofern der Tumor Hormonrezeptoren aufweist, kann oft zunächst eine antihormonelle Therapie gewählt werden. Ein solcher Behandlungsansatz ist meist auch nach einer antihormonellen Vorbehandlung möglich. Erst wenn die antihormonellen Therapieverfahren nicht mehr ausreichend wirksam sind, oder wenn keine Hormonrezeptoren auf den Tumorzellen vorliegen, oder ein rasches Tumorfortschreiten vorliegt und wichtige Körperfunktionen bedroht sind, wird eine Chemotherapie (eventuell unter Einschluß von Herceptin) durchzuführen sein.
Welche Arten von Chemotherapie werden verwendet ?
In Betracht kommen 3-wöchentliche intravenöse Therapien, wöchentliche intravenöse Therapien in geringerer Dosis, Tablettentherapien, die Gabe von Einzelmedikamenten oder von Kombinationsbehandlungen. Die Wahl der Behandlung erfolgt in einem gemeinsamen Gespräch mit der Patientin unter Berücksichtigung des Krankheitsverlaufs, der Tumorausdehnung, den Begleiterkrankungen, der Vorbehandlung sowie individuellen, persönlichen Lebensumständen. Gelegentlich kommen begleitende Therapieverfahren hinzu, wie beispielsweise eine Strahlentherapie bei schmerzhaften oder frakturgefährdenden Knochenmetastasen. In diesen Fällen ist eine enge Absprache erforderlich, um Chemo- und Strahlentherapie miteinander zu koordinieren.
Wie lange wird die Therapie fortgeführt ? Gibt es längere Therapiepausen ?
Prinzipiell gilt, dass eine möglichst langfristige Kontrolle der Tumorerkrankung auch eine langfristig angelegte Behandlung beinhaltet. Auch hier gilt ein Behandlungsgrundsatz wie bei chronischen Erkrankungen, die einer kontinuierlichen, lebenslangen Behandlung bedürfen. Sofern eine gute Kontrolle der Erkrankung erreicht ist beispielsweise durch Verkleinerung oder Wachstumsstillstand von Metastasen, kann überlegt werden, ob eine Therapiepause sinnvoll ist oder ob die Behandlungsintensität eventuell verringert werden kann. Dies kann vielleicht durch eine Verlängerung von Therapieintervallen, durch einen Übergang von einer Chemotherapie auf eine antihormonelle Therapie oder von einer Kombinationschemotherapie auf eine Einzelmedikamententherapie erreicht werden.
Sind Urlaube möglich ?
Sofern eine aktuell stabile Tumorsituation vorliegt, können fast immer Urlaube geplant und durchgeführt werden. Diese sind meist auch sehr sinnvoll, um zu einer körperlichen und psychischen Erholung und Stabilisierung nach einer vielleicht zwischenzeitlich intensiveren Behandlungsphase zu führen. Urlaube sollten daher aktiv geplant und mit den voraussichtlichen Zeitplänen einer medikamentösen Behandlung abgestimmt werden.
Wer sollte die Behandlung durchführen ?
Eine Chemotherapie bei metastasierter Erkrankung sollte durch besonders erfahrene, hauptamtlich in der medikamentösen Tumortherapie tätige Ärzte durchgeführt, gesteuert und überwacht werden. Im Gegensatz zu zahlreichen europäischen Nachbarländern und den USA, wo überwiegend medizinische Onkologen für diese Therapie verantwortlich sind, ist die Durchführung einer Chemotherapie - auch bei Patienten/Innen mit einer metastasierten Erkrankung - in Deutschland jedoch nicht einer spezialisierten medizinischen Disziplin vorbehalten, ebensowenig wie die Begriffe Onkologie und Onkologe nicht an eine Spezialisierung gebunden sind. Fachärzte mit einer ausschließlichen Spezialisierung auf die medikamentöse Tumorbehandlung sind in Deutschland die "Fachärzte für internistische Onkologie und Hämatologie", entsprechend den o.g. medizinischen Onkologen. Entscheidend sind die umfangreiche, langjährige Erfahrung mit der Erkrankung, den Wirkungen und Nebenwirkungen der Tumormedikamente, die Berücksichtigung von Begleiterkrankungen, die vor allem bei älteren Patienten bedeutsam sein können und für das Gesamtbehandlungskonzept zu berücksichtigen sind sowie spezielle Kenntnisse in der unterstützenden (suppoprtiven) Behandlung von Begleiterscheinungen der Tumorerkrankung und der Behandlungsnebenwirkungen.